人类的旅程,是不断失败、不断开拓。
一个健康的人,他可能有很多愿望—享受美食、环游世界,感受快乐;而一个病人,只有一个。
2024年7月22日至26日,第 25 届国际艾滋病大会(AIDS 2024)在德国慕尼黑召开,同时,前段时间沸沸扬扬的全球第 7 例 HIV 治愈者“第二位柏林病人”的详细情况,也在此会议上公布。
该患者不愿透露个人信息,故而我们无法得知他的姓名。已知的信息是,其为一名成年男性,是目前所有公开报道中,世界上第七个在干细胞移植后治愈艾滋病毒的人。
与前六例 HIV 治愈案例一致,第二位柏林病人和他们一样,是通过造血干细胞移植实现的 HIV 治愈。
而与“第一位柏林病人”,也就是首位艾滋病治愈者Timothy Ray Brown,乃至其他所有艾滋病治愈者不同的是,他还是首位干细胞捐献者具有单一而非双重CCR5-delta32突变的HIV治愈病例。
这是否意味着更具普适性、通用性的HIV治疗策略变得可及了?
01
治疗过程披露
该患者的患病以及治疗经过,我们用一条时间轴来表述:
2009年:患者首次被检测出HIV阳性。
2015年:患者被确诊为急性髓系白血病(AML)。
2015年末:患者接受了造血干细胞移植的治疗。
2018年9月:患者中断了抗逆转录病毒疗法(ART)的使用。
2018年9月至接下来的五年半时间:HIV病毒并未出现复发的情况。
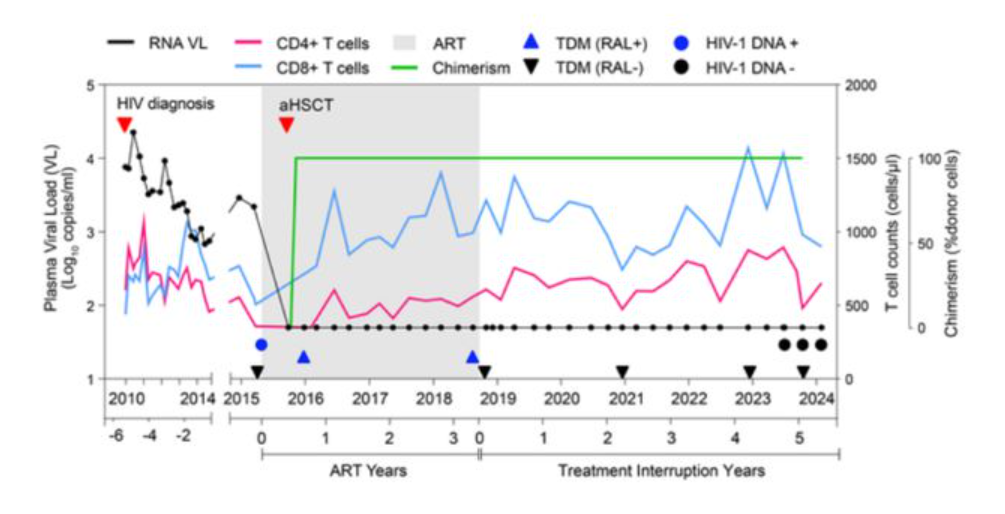
回看过去个位数的治愈病例,我们不难发现其共通之处—均为通过造血干细胞移植实现的治愈,再深挖一点,这些治愈病例移植的干细胞均含有一种罕见的CCR5-delta32基因突变。
我们上文说到,“第二位柏林病人”的干细胞捐献者具有单一而非双重CCR5-delta32突变,这在医学上意味着什么,必须详细分析。
02
治愈艾滋的基因
先说CCR5,其在HIV感染过程中扮演着关键角色。
HIV进入人体并破坏人体免疫细胞CD4+T之前,需要先经过一道迷宫,迷宫很复杂,需要一个“导游”,CCR5就是主要“导游”之一。

然后,当CCR5编码基因发生突变,第32对碱基缺失时,即产生了CCR5-delta32突变基因。这种突变导致基因无法编码成熟的CCR5,因此CD4+T细胞表面无CCR5存在,HIV没有“导游”带着,就无法识别并通过其进入细胞,达到复制和破坏细胞的目的。
因此,可以说,有CCR5-delta32突变基因,就代表着对艾滋病有先天的免疫力(虽然不太准确,但是可以体现CCR5-delta32突变基因的重要性)。
当捐赠者遗传了来自父母双方的 CCR5-delta32 突变,即为纯合子,基本上对HIV具有免疫力。
在此前的HIV治愈者中,所有捐赠造血干细胞者均携带纯合CCR5-delta32突变基因,因此,这类型的人的造血干细胞移植被普遍认为能达到理想的治疗效果。但是,纯合子的供者相对稀缺,这限制了该治疗方法的应用范围。
当供者父母中只有一人携带CCR5-delta32突变时,便是杂合子,即供者有一半是CCR5,对艾滋病无先天的免疫,一半是CCR5-delta32突变,对艾滋有抵抗作用。
二者综合起来就等于:理论上无法做到对 HIV 免疫,还是会得艾滋病,但疾病发展会相对缓慢很多。
“第二位柏林病人”接受的就是杂合CCR5-delta32造血干细胞移植,他本人也是杂合 CCR5-delta32 突变携带者。
这一案例证明,即使存在病毒可以识别的功能受体,治愈HIV也是可能的。这可能是由于供者免疫细胞已经消除了患者所有感染HIV的细胞,使病毒无法再感染供者来源的新细胞。
这一案例背后的意义则是,它扩大了潜在供者的范围,因为具有杂合突变的人明显多于纯合突变的人。没有到全人类层面上的治愈,但确实拓宽了治愈策略。
03
不容忽视的严峻
联合国艾滋病规划署的经济学家埃里克·拉蒙塔涅主导了一项新研究,估算了114个国家未能实现“95-95-95”目标可能带来的人力与经济负担。
“95-95-95”目标是指95%的艾滋病毒感染者了解自己的感染状况,95%的已知感染者正在接受抗逆转录病毒治疗,以及95%的接受治疗者体内病毒得到有效抑制。
研究对比了实现该目标与“维持现状”(即将艾滋病毒相关服务的覆盖率保持在2020年的水平直至2050年)两种情境下的成本、效益及经济回报。
结果显示,若全球目标无法实现,预计2021年至2050年间将有大量新增艾滋病毒感染和与艾滋病相关的死亡,且人均经济成本将大幅增加:所有低收入和中等收入国家的人均经济成本预计将达8291美元,而维持现状的人均成本则为670美元。
世界正处于应对艾滋病毒的关键时刻,倘若毫无动作,面临的风险是极高的。
事实上,考虑到艾滋病的治愈难度,十几年来,艾滋病治愈案例并不算少了,但仍然无法做到在全人类层面上战胜它,尽管已经有多例成功在前,干细胞移植仍然不具备普适性,只有在非常严重的情况下才能被考虑:同时患有白血病和艾滋病,具有CCR5-delta32突变基因,且不论能同时满足以上条件有多难,真患上这两种疾病,能够熬过正式移植干细胞之前的预处理者少之又少。
End
写在文末

但人类的旅程是不断失败、不断开拓的旅程,现在的我们可能很难做到治愈艾滋病,但相比之前的“无法治愈”,我们毫无疑问已然迈上了新的台阶,第5例艾滋病治愈者透露出的老年患者治愈可能性、第6例患者的不含 CCR5-delta32 干细胞移植,都是我们抬起脚步的动力。
